Περιμένοντας τoν... ΕΜΑ και το εμβόλιο - Ρεπορτάζ του Κώστα Αργυρού
O ρόλος του Ευρωπαϊκού Οργανισμού Φαρμάκων, η κυλιόμενη αξιολόγηση, η διαδικασία ταχείας έγκρισης, και ο αγώνας ταχύτητας για το πρώτο εμβόλιο κατά του κορωνοϊού.
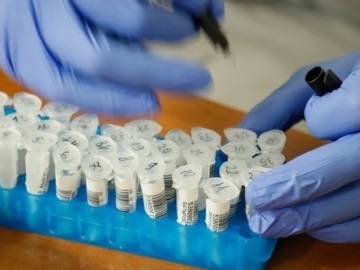
H κούρσα για αποτελεσματικά εμβόλια κατά του κορονωϊού ανεβάζει πλέον ταχύτητες. Η αμερικανική φαρμακευτική εταιρεία Moderna θέλει να είναι η πρώτη εταιρεία, που θα υποβάλει αίτηση έγκρισης για αντίστοιχο εμβόλιο στην ΕΕ. Αλλά πώς γίνεται η διαδικασία έγκρισης εμβολίου στην Ευρώπη;
Σήμερα ουσιαστικά κανένα εμβόλιο δεν έχει εγκριθεί αποκλειστικά για την αγορά της Ευρώπης.
Η έγκριση ενός εμβολίου ρυθμίζεται σε μεγάλο βαθμό από τη λεγόμενη κεντρική ευρωπαϊκή διαδικασία. Ο κεντρικός οργανισμός δοκιμών είναι ο Ευρωπαϊκός Οργανισμός Φαρμάκων (EMA) που ιδρύθηκε το 1995 και εδρεύει στο Άμστερνταμ. Ο ΕΜΑ εγγυάται την επιστημονική αξιολόγηση, την εποπτεία και την παρακολούθηση της ασφάλειας φαρμάκων για τους ανθρώπους και τα ζώα στην ΕΕ. Μετά από μια αρχική δοκιμή, η Επιτροπή Φαρμάκων για Ανθρώπινη Χρήση (CHMP) εκδίδει στη συνέχεια σύσταση σχετικά με την αίτηση έγκρισης. Αυτό αποτελεί τη βάση για την τελική απόφαση έγκρισης από την Ευρωπαϊκή Επιτροπή.
Αυτό που ζητούν τώρα οι υποψήφιες εταιρίες είναι μια ταχεία διαδικασία έγκρισης λόγω της covid-19. Aυτό σημαίνει ότι τα υποψήφια εμβόλια μπορούν να αξιολογηθούν σε μια λεγόμενη κυλιόμενη αξιολόγηση (Rolling Review). Ο στόχος είναι να επιταχυνθεί η αξιολόγηση των φαρμάκων από τον ΕΜΑ.
Ουσιαστικά η αξιολόγηση του εμβολίου ξεκινά προτού υποβληθούν όλα τα δεδομένα, που απαιτούνται για μια «κανονική» αίτηση έγκρισης. Ωστόσο, σύμφωνα με τον ΕΜΑ, διασφαλίζεται ότι οι απαιτήσεις για την ποιότητα, την ασφάλεια και την αποτελεσματικότητα των ενδιαφερόμενων υποψήφιων εμβολίων θα παραμείνουν υψηλές. Η αμερικανική φαρμακευτική εταιρεία Moderna θα υποβάλει τώρα αίτηση για έγκριση για το εμβόλιο κορωνοϊού στην ΕΕ. Ταυτόχρονα, υποβάλλεται αίτηση για έγκριση έκτακτης ανάγκης στις ΗΠΑ. Επομένως, η κυλιόμενη διαδικασία επανεξέτασης θα εφαρμοστεί τόσο στο εμβόλιο Moderna όσο και στο εξαιρετικά ελπιδοφόρο εμβόλιο από την Biontech/PQzer.
Τι ακριβώς ελέγχει ο ΕΜΑ κατά τη διαδικασία έγκρισης; Σύμφωνα με τη νομοθεσία της ΕΕ για τα ναρκωτικά, τα οφέλη ενός εμβολίου Covid-19 πρέπει να είναι πολύ μεγαλύτερα από οποιεσδήποτε παρενέργειες ή πιθανούς κινδύνους. Η Επιτροπή Φαρμάκων για Ανθρώπινη Χρήση, μαζί με επιστήμονες
από όλες τις ευρωπαϊκές ρυθμιστικές αρχές, είναι υπεύθυνη για την αξιολόγηση ενός νέου προϊόντος. Οι ειδικοί παρέχουν αξιολογήσεις της επίδρασης του φαρμάκου και σχολιάζουν τις αβεβαιότητες των δεδομένων. Μπορούν επίσης να υποβάλουν στον αιτούντα επιπρόσθετες ερωτήσεις.
Η Επιτροπή Αξιολόγησης Κινδύνων Φαρμακοεπαγρύπνησης (PRAC) αξιολογεί την ασφάλεια των ναρκωτικών.
Πόσος χρόνος χρειάζεται όμως μέχρι την τελική έγκριση εμβολίου; Ο ΕΜΑ δεν έχει κάνει καμιά σαφή δήλωση σχετικά με αυτό το ζήτημα.
Δεδομένου ότι οι φάσεις ανάπτυξης των υποψηφίων εμβολίων παρακολουθώνταν από την αρχή στην κυλιόμενη αξιολόγηση, ο ΕΜΑ έχει ήδη μια εικόνα για την πορεία των ερευνών και τα αποτελέσματά της. Σύμφωνα με εκπρόσωπο της, η τελική απόφαση της Κομισιόν είναι συνήθως τυπικό θέμα. Στην περίπτωση του υποψηφίου εμβολίου της Moderna, το αιτούμενο είναι «ταχεία απόφαση» για αδειοδότηση υπό όρους.
Η λεγόμενη έγκριση υπό όρους προορίζεται να ικανοποιήσει επείγουσες ιατρικές ανάγκες. Τα δεδομένα που λείπουν, όπως η μακροπρόθεσμη αποτελεσματικότητα, πρέπει να υποβάλλονται το συντομότερο δυνατό σύμφωνα με τις απαιτήσεις έγκρισης. Η έγκριση υπό όρους ισχύει για ένα έτος, αλλά μπορεί επίσης να παραταθεί. Αυτός ο τύπος έγκρισης προορίζεται για τα περισσότερα εμβόλια κατά του κορωνοϊού, τα οποία δεν έχουν μακροχρόνιο ιστορικό. Όταν οι χώρες θέλουν να ξεκινήσουν τον εμβολιασμό κάθε μια από αυτές έχει την αντίστοιχη αρχή, η οποία θα δώσει την σχετική εθνική άδεια για να κυκλοφορήσει το φάρμακο και να αρχίσουν οι εμβολιασμοί.